Причина одинакового количества элементов в первых трех периодах химического ряда
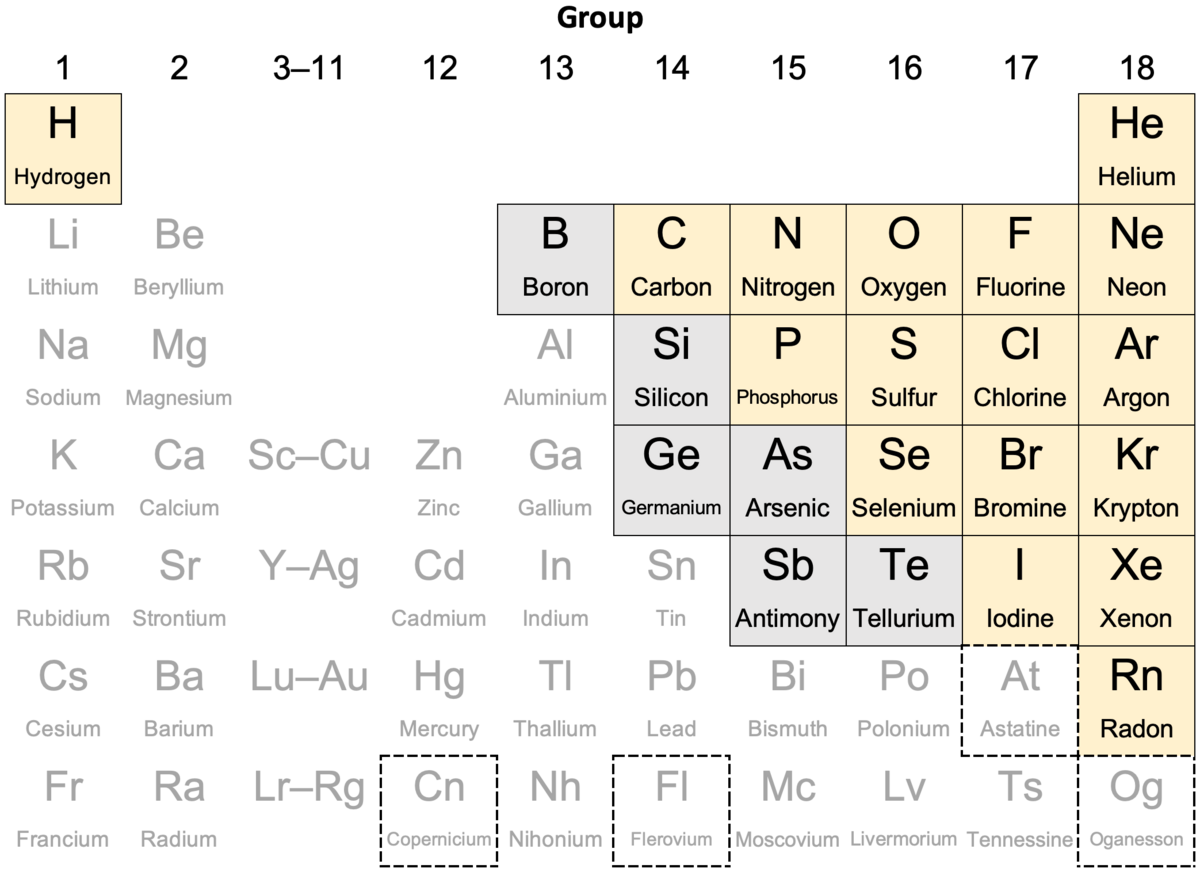
Периодическая система химических элементов является одной из самых важных основ науки о химии. На первый взгляд, расположение элементов в таблице Периодической системы может показаться случайным, но на самом деле оно имеет глубокий смысл и объясняется определенными закономерностями.
Один из главных вопросов, возникающих при изучении периодической системы, — почему в первых трех периодах ряду 2 8 8 именно такое соответствие числа элементов? Для ответа на этот вопрос необходимо обратиться к строению атомов и электронной конфигурации.
Каждый атом состоит из ядра и облака электронов, которое окружает его. Главная оболочка определяет электронную конфигурацию атома и состоит из нескольких подоболочек, каждая из которых может содержать определенное количество электронов. Как правило, количество электронов в каждой подоболочке равно сумме квадратов натуральных чисел от 1 до номера подоболочки.
Причина соответствия числа элементов в первых трех периодах ряда 2 8 8
Ряд 2 8 8 относится к системе расположения химических элементов в периодической таблице Менделеева. В первых трех периодах этого ряда находится соответственно 2, 8 и 8 элементов. Эта закономерность обусловлена строением электронных оболочек атомов и их стремлением к достижению наиболее устойчивой электронной конфигурации.
В первом периоде находится всего два элемента: водород (H) и гелий (He). Оба этих элемента имеют всего одну электронную оболочку, на которой расположен соответственно один и два электрона. Этот период соответствует заполнению первой электронной оболочки атомом, что придает им особую устойчивость.
Во втором периоде находятся восемь элементов: литий (Li), бериллий (Be), бор (B), углерод (C), азот (N), кислород (O), фтор (F) и неон (Ne). У этих элементов вторая электронная оболочка заполняется последовательно, начиная с элемента литий, который имеет 3 электрона, и заканчивая элементом неон, у которого 10 электронов. Для этих элементов заполнение второй электронной оболочки до 8 электронов придает им стабильность и химическую инертность.
В третьем периоде также находится восемь элементов: натрий (Na), магний (Mg), алюминий (Al), кремний (Si), фосфор (P), сера (S), хлор (Cl) и аргон (Ar). Для этих элементов третья электронная оболочка заполняется последовательно, начиная с элемента натрий, который имеет 11 электронов, и заканчивая элементом аргон, у которого 18 электронов. Заполнение третьей электронной оболочки до 8 электронов также придает этим элементам устойчивость и химическую инертность.
Таким образом, соответствие числа элементов в первых трех периодах ряда 2 8 8 определяется строением электронных оболочек атомов и стремлением элементов к достижению наиболее стабильной и устойчивой электронной конфигурации.
Соответствие числа элементов первых трех периодов
Первый период включает два элемента: водород и гелий. Второй период состоит из восьми элементов: лития, бериллия, бора, углерода, азота, кислорода, фтора и неона. Третий период также содержит восемь элементов: натрия, магния, алюминия, кремния, фосфора, серы, хлора и аргона.
Такое соответствие числа элементов в первых трех периодах объясняется принципом заполнения энергетических уровней электронами. Каждому периоду соответствует заполнение одного энергетического уровня. В первом периоде заполняется первый энергетический уровень с одним электроном. Во втором периоде заполняется второй энергетический уровень, который может вместить восемь электронов. Третий период соответствует заполнению третьего энергетического уровня, который также может вместить восемь электронов.
Первый период: Малый размер атомов
Малый размер атомов обуславливается наличием только одной электронной оболочки, которая может содержать всего два электрона. Атом водорода имеет всего один электрон, занимающий единственную энергетическую оболочку. Атом гелия, в свою очередь, имеет два электрона, которые также располагаются на первой энергетической оболочке.
Малый размер атомов первого периода связан с тем, что чем меньше атом, тем ближе его электроны к ядру, что приводит к более сильному притяжению электронов ядром. Это объясняет стабильность этих элементов и отсутствие необходимости заполнять большее количество энергетических оболочек.
Малый размер атомов также связан с электронной конфигурацией элементов первого периода. Водород и гелий имеют электронную конфигурацию 1s^1 и 1s^2 соответственно, что указывает на заполнение первой энергетической оболочки. Благодаря такой конфигурации, атомы водорода и гелия имеют минимальный размер в периодической системе.
| Элемент | Атомный номер | Электронная конфигурация |
|---|---|---|
| Водород (H) | 1 | 1s^1 |
| Гелий (He) | 2 | 1s^2 |
Второй период: Возможность образования двойных связей
Второй период в ряду элементов (Li, Be, B, C, N, O, F, Ne) характеризуется возможностью образования двойных связей. Элементы этого периода имеют валентность, равную двум или более, что позволяет им образовывать связи, в которых участвует более одной пары электронов.
Образование двойных связей является результатом несыщущего электронного строения атомов второго периода. Например, атом углерода имеет 4 валентных электрона и образует четыре связи в молекуле метана (CH4). В одной из этих связей участвуют две пары электронов, образуя двойную связь между углеродом и одним из атомов водорода.
Такое поведение элементов второго периода обусловлено их стремлением к достижению стабильного электронного строения, в котором внешняя оболочка содержит полный комплект валентных электронов. Образование двойных связей позволяет элементам второго периода насытить валентную оболочку и достичь более стабильного положения.
Третий период: Появление дополнительных энергетических уровней
На третьем энергетическом уровне могут находиться до 18 электронов, что делает третий период самым большим по размеру из первых трех периодов. Это объясняет повышение количества элементов в этом периоде по сравнению с предыдущими.
Таким образом, третий период характеризуется появлением дополнительных энергетических уровней для размещения электронов, что приводит к соответствующему увеличению числа элементов в периоде.
Вопрос-ответ:
Почему в первом периоде ряда элементов ионный радиус увеличивается слабее, чем межатомный радиус?
В первом периоде ряда на каждое последующее значение заряда каждого иона требуется добавлять по одному электрону, что приводит к увеличению эффективного заряда ядра и сужению ионного радиуса.
В чем заключается причина того, что число элементов во втором и третьем периодах одинаковое?
Во втором и третьем периодах ряда, первая и вторая энергетические оболочки заполняются полностью, что приводит к одинаковому числу элементов в данных периодах.
Почему количество электронов в атомах элементов в первом периоде ряда не совпадает с их зарядом?
В первом периоде ряда энергетическая оболочка может вместить только два электрона. При этом атомы элементов в данном периоде имеют разное число электронов, недостающие электроны отсутствуют в первой энергетической оболочке.
Почему в первом периоде ряда число элементов составляет только 2?
В первом периоде ряда на данном уровне заполняется только первая энергетическая оболочка (K), которая вмещает не более 2 электронов.
Каким образом определяется число элементов в каждом периоде ряда?
Число элементов в каждом периоде ряда определяется числом энергетических уровней, а также заполнением электронных оболочек и подуровней. Каждый период соответствует заполнению нового энергетического уровня.
Почему в первом периоде ряда 2 8 8 только 2 элемента?
В первом периоде ряда 2 8 8 находятся элементы с самыми низкими атомными номерами. Периодическая система химических элементов состоит из элементов, расположенных в порядке возрастания их атомных номеров. Первый период начинается с водорода, а затем идет гелий. Поэтому в первом периоде только два элемента.